MPQ模块在CHO细胞蛋白组学中的研究进展
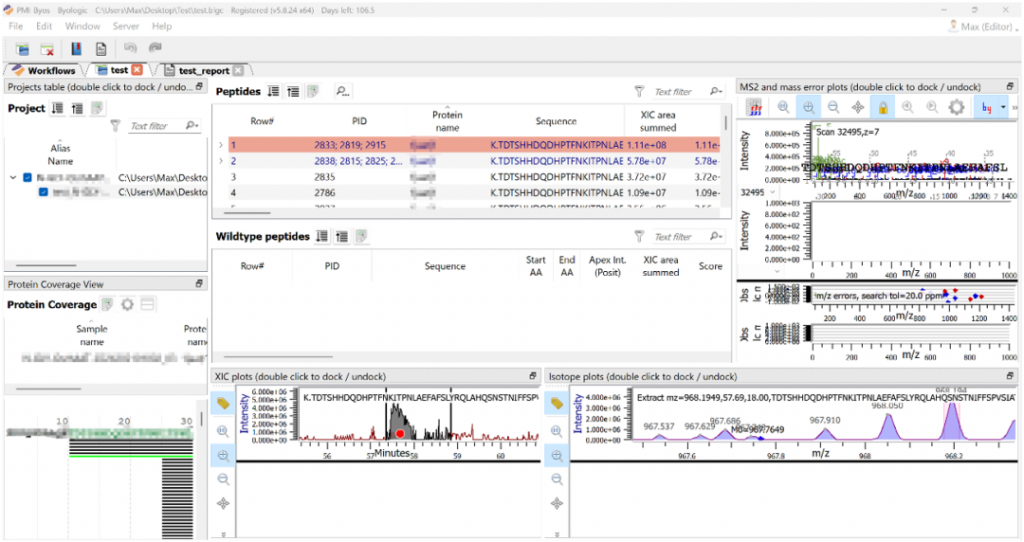
前言 INTRODUCTION 在生物制药开发过程中,对中国仓鼠卵巢 (CHO) 细胞进行蛋白质组学研究,在药物纯度验证和分析中是至关重要的。全新的多蛋白定量 (MPQ module) 质谱分析工作流程工具将使生物制药研发各个阶段的蛋白质科学家受益。MPQ模块中包含的不同workflow提供了一个全面的框架,可快速鉴定和定量分析复杂CHO混合物中的数千种蛋白质,并采用以蛋白质为中心的高效布局。这个方法简化了从早期细胞系开发到最终分析阶段的流程,最终提高了生物制药开发中蛋白质分析的整体效率和可靠性。 方法 METHODS 本研究使用通用蛋白质组学标准1和2 (UPS1/2) 以及等量的CHO细胞蛋白质组加标物 (spike-in) 对48种蛋白质进行非标记定量分析。样品经过消化,并被处理为单个组分或多个组分。接着,对各种液质联用 (LC-MS) 方法(特别是数据依赖性采集 (DDA))的横向对比,则是侧重于对诸如速度、鉴定出的蛋白质和肽段数量、缺失值的发生率以及定量水平等指标的比较。关注点包括上述提及的48种UPS蛋白质与CHO蛋白质的理论比值和观测比值。 图1. 包含2种不同条件的所有样本检查视图,使用运行间匹配,对8个样本中不同保留时间的肽段鉴定结果,并使用提取离子流色谱图 (XIC) 进行比对。v5.8 版本新增了“以蛋白质为中心的视图”,使分析人员能够快速筛选和查询特定蛋白质。 检查视图以及自动生成的报告,可通过分析质谱仪的精度、分辨率和酶消化效率,快速评估样品制备质量。 图2. 将通用蛋白质组学标准品1和2中的46种蛋白质(共48种)加入CHO蛋白质组中,测得其相对丰度。 (A) 在等量CHO细胞(包括重复样品)混合的样品中,检测到分子量为6,000至83,000道尔顿的人类蛋白质(每种5 pmol)。相对蛋白质丰度(以百分比表示)反映了CHO蛋白质组实验中,仪器检测和软件识别的差异。 (B) 将48种人类蛋白质的相同复杂混合物制备成浓度动态范围从500 pmol到50 pmol的样品,在与50 pmol CHO蛋白质组(包括重复样品)混合的样品中,也检测到了46种蛋白质,且浓度范围较大。结果表明,仪器检测和软件识别的动态范围符合预期。 图3. 分馏和单次采集条件下蛋白质丰度比较的火山图。 (A) USP1样品的倍数变化范围为2到4,表明从单次采集到分馏数据采集条件,丰度显著增加。 (B) 在USP2样品中,大多数检测到的蛋白质的倍数变化范围为-6到+4,这反映出分馏采集的丰度变化比单次采集的丰度变化更大,这表明由于复杂样品中的离子抑制效应,分馏可以提高检测灵敏度。 结论 CONCLUSION Byosphere中的MPQ module为CHO蛋白质组学研究提供了一种快速、准确且全面的方法。 适用于广泛的生物制药应用,支持更快、更可靠的决策。 持续改进蛋白质组学分析,为工艺开发和法规遵从做出重大贡献。 致谢 感谢强生创新医药和Protein Metrics LLC团队成员的合作与贡献。 作者 Alex Zhai¹², Ilker …