
MAM是一种基于LC-MS的肽图分析方法,近年来在蛋白质治疗药物行业得到了广泛应用。由于MAM能够识别并靶向定量多个关键质量属性(CQAs),此次参与MAM循环比对的研究人员,购买了未消化的市售NIST mAb及获得了胰蛋白酶消化的市售NIST mAb。
对获取的数据进行收集和分析,旨在评估不同实验室间测量方法和样品制备方法的可重复性。本次实验室间MAM研究的目的是确认并改进各实验室用于抗体治疗药物MAM分析的基本技术。
方法

Sample ①
NIST mAb (NIST, RM 8671);
各实验室进行胰蛋白酶消化
Sample ②
NIST mAb胰蛋白酶消化标准肽段;
(Waters 186009126) 浓度为 0.2mg/mL
各实验室使用相同的色谱及质谱,并且液相和质谱的方法也保持一致。1
1. Nat Protoc. 2023 Apr;18(4):1056-1089

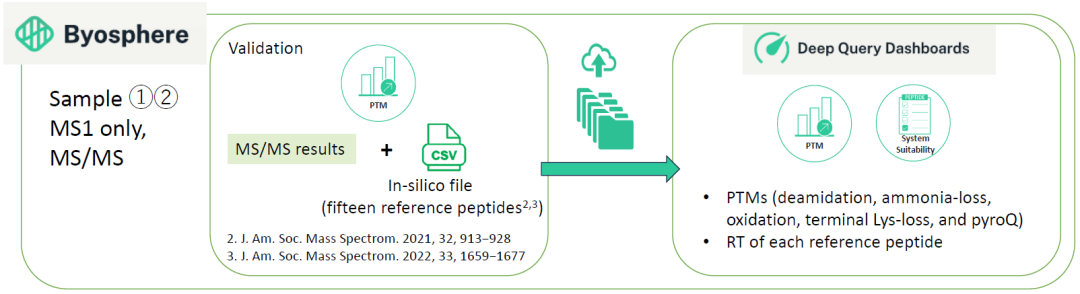
结果

参考肽段的相对峰面积、质量准确度和保留时间的比较
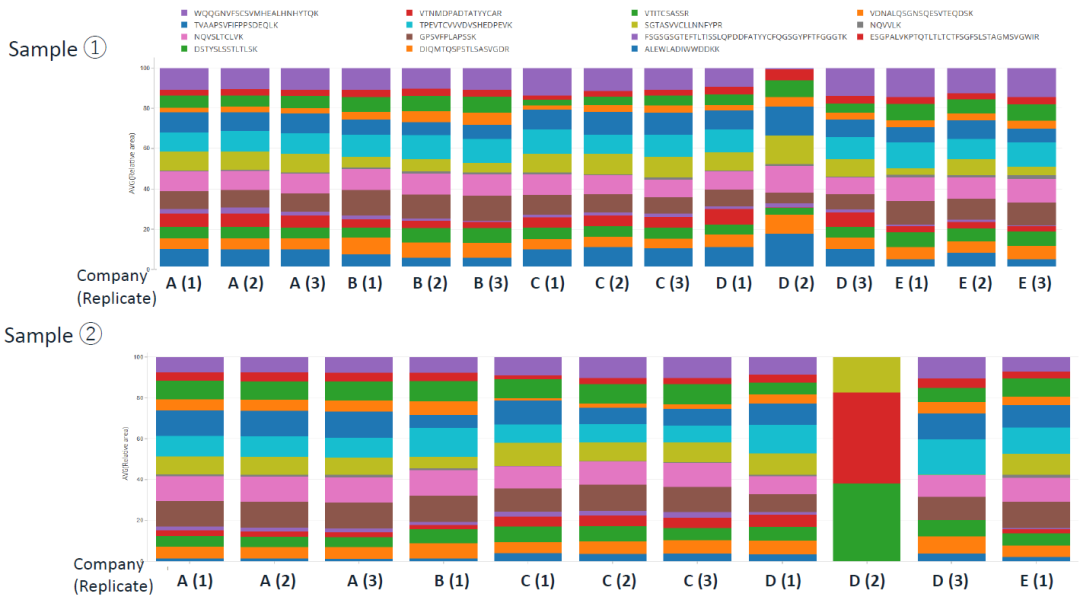
图1. 参考肽段的相对峰面积(仅MS1数据)
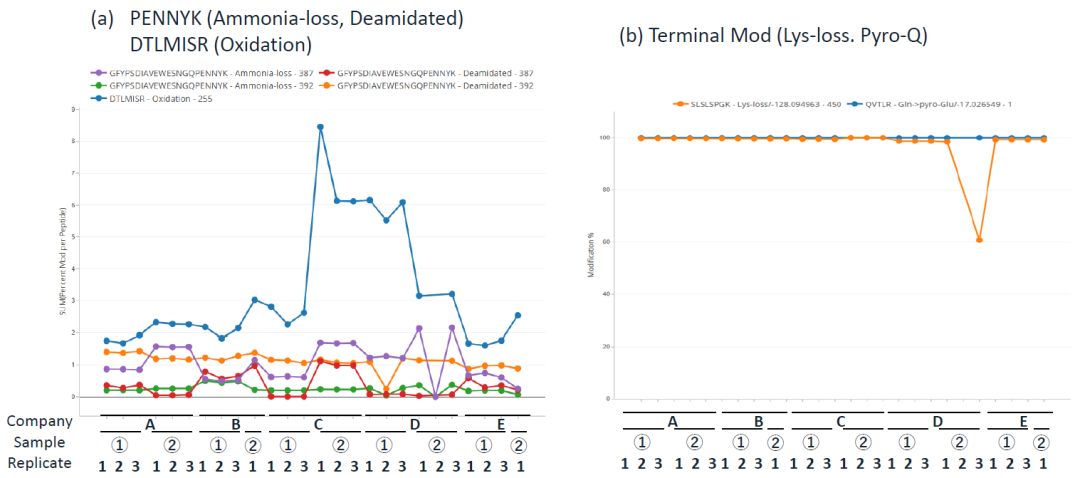
图2. 修饰比例 (%) (仅MS1数据)
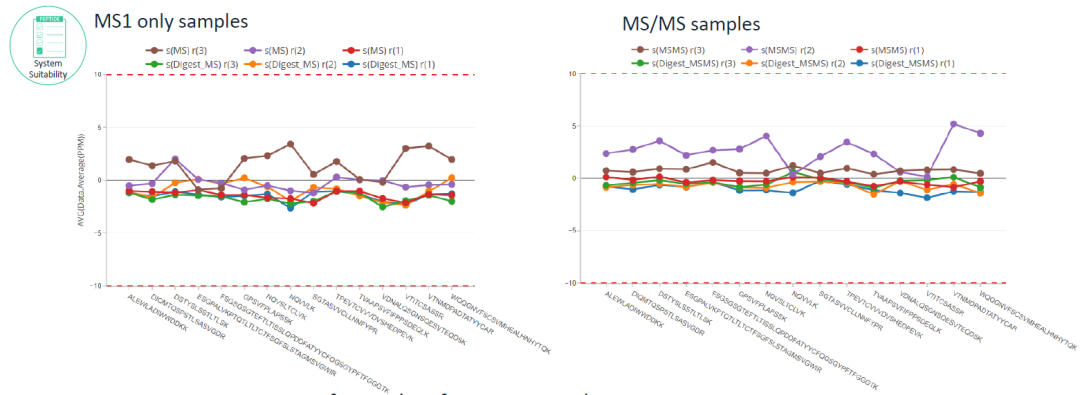
图3. 各参考肽段的平均质量准确度(单位: ppm)
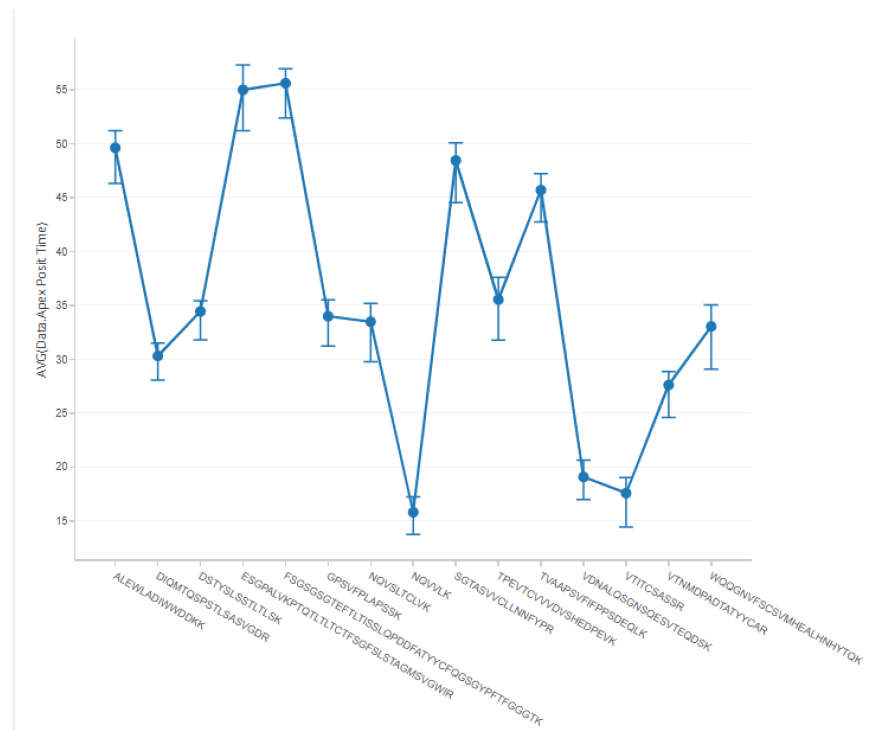
图4. 各参考肽段的保留时间变化
肽段DTLMISR氧化修饰的百分比总和在两个实验室的数据中存在一些异常值。而对于脱酰胺化的‘PENNY’肽段,其修饰百分比总和并未显示出任何异常值。
有一个实验室针对所购已消化样品的数据出现了异常值,然而,其他参与者的数据中保留时间的重现性相似。这表明本研究中的数据足以用于比较。
结论

对于在日本开展的MAM循环研究,使用独立液相色谱和质谱系统对购买的和内部消化的NIST mAb进行了分析,这些系统仅在MS1模式以及MS/MS模式下获取数据。我们使用Byosphere比较了几种预定义的参考NIST mAb关键质量属性(CQAs) (脱酰胺、氧化、末端赖氨酸丢失和焦谷氨酸化) 的相对丰度。鸟瞰图使研究人员能够快速发现异常值,并改进样品制备、质谱参数和分离条件。
Byosphere的Dashboard功能使用户能够查看不同样本和实验室中的肽修饰率及系统适用性,并能够从大量数据中获得洞察。
作者
Ayako Kurimoto, K. Ilker Sen
Protein Metrics, LLC, Boston, MA
致谢及利益冲突声明
作者谨向日本国立材料科学研究所 (NIMS) 的Kohsaku Kawakami博士以及参与材料开放平台(MOP) 药物科学的制药公司表示感谢。
作者为Protein Metrics, LLC公司的员工,该公司已将此处描述的软件商业化。
END
往期推荐


